

Liposomalne suplementy diety w ostatnich latach stały się jedną z najczęściej omawianych technologii w świecie suplementów diety.
Technologia liposomalna stała się w ostatnich latach jednym z najczęściej używanych określeń w świecie suplementów diety. Na rynku pojawia się coraz więcej produktów opisywanych jako liposomalne — od witaminy C, przez witaminy z grupy B, aż po ekstrakty roślinne i związki o niskiej rozpuszczalności.
Jednocześnie coraz częściej spotykamy dwa różne podejścia technologiczne:
- płynne formulacje liposomalne,
- proszki określane jako liposomalne.
Na pierwszy rzut oka oba rozwiązania mogą wydawać się podobne. W praktyce jednak różnica między nimi jest istotna — zarówno z punktu widzenia technologii, jak i późniejszej jakości produktu.
Warto więc zadać sobie podstawowe pytanie: czy każdy suplement określany jako liposomalny działa w ten sam sposób?
Czym jest liposom? Krótka budowa
Liposom to mikroskopijna struktura zbudowana z fosfolipidów, czyli cząsteczek, które mają dwie różne części:
- część hydrofilową, czyli „lubiącą wodę”,
- część lipofilową, czyli „lubiącą tłuszcz”.
Dzięki temu fosfolipidy w środowisku wodnym spontanicznie układają się w podwójną warstwę lipidową. Powstaje wtedy mały pęcherzyk, którego środek stanowi faza wodna, a zewnętrzną granicę — błona fosfolipidowa.
To właśnie taka struktura nazywana jest liposomem.
W praktyce oznacza to, że liposom może pełnić rolę nośnika dla różnych substancji:
- hydrofilowych, które mogą znaleźć się we wnętrzu wodnym,
- lipofilowych, które mogą wiązać się z warstwą lipidową.
To rozwiązanie nie jest czymś oderwanym od natury. Układy lipidowe są organizmowi dobrze znane, ponieważ przypominają budową błony komórkowe. Właśnie dlatego technologia liposomalna budzi tak duże zainteresowanie w obszarze suplementów i formulacji bioaktywnych składników.
Dlaczego liposomy zwiększają biodostępność
Popularność liposomów wynika z jednego kluczowego powodu: mogą poprawiać biodostępność substancji aktywnych.
Biodostępność to w uproszczeniu stopień, w jakim dany składnik zostaje wchłonięty i staje się dostępny dla organizmu. Sama obecność substancji w kapsułce, proszku czy płynie nie oznacza jeszcze, że organizm rzeczywiście ją wykorzysta.
W przypadku dobrze zaprojektowanej formulacji liposomalnej korzyści mogą wynikać z kilku mechanizmów:
- ochrony składnika aktywnego przed częściową degradacją,
- łatwiejszego kontaktu z błonami biologicznymi,
- lepszej dyspersji w środowisku wodnym,
- zwiększenia powierzchni kontaktu dzięki małym rozmiarom cząstek.
To szczególnie istotne przy składnikach, które w klasycznej formie mają słabą rozpuszczalność lub ograniczone wchłanianie.
Dwie główne technologie liposomalne na rynku
Choć wiele produktów używa tego samego określenia marketingowego, w praktyce na rynku funkcjonują dwa różne modele technologiczne.
Płynne formulacje liposomalne
W tym przypadku liposomy lub dyspersja lipidowa istnieją już w gotowym produkcie. Oznacza to, że producent przygotowuje układ w fazie wodnej i stabilizuje go jeszcze przed podaniem klientowi.
To właśnie taki produkt można realnie zbadać jako gotową formulację.
Proszki określane jako liposomalne
W tej grupie najczęściej nie mamy do czynienia z gotowymi liposomami obecnymi w fazie wodnej. Zwykle jest to suchy układ zawierający:
- składnik aktywny,
- fosfolipidy,
- czasem substancje pomocnicze.
Po dodaniu wody lub po kontakcie z płynami przewodu pokarmowego taki proszek może tworzyć struktury lipidowe, które mają przypominać układ liposomalny.
I właśnie tu pojawia się najważniejsza różnica:
w produkcie płynnym jakość układu można ocenić od razu, natomiast w proszku rzeczywisty układ powstaje dopiero później.
Jak powstają płynne liposomy
Płynna formulacja liposomalna powstaje w środowisku wodnym. W zależności od technologii wykorzystuje się odpowiednio dobrane:
- fosfolipidy,
- fazę wodną,
- parametry mieszania,
- temperaturę,
- energię homogenizacji lub sonikacji.
Celem jest uzyskanie możliwie jednorodnej dyspersji o kontrolowanym rozmiarze cząstek i odpowiedniej stabilności.
Największą zaletą tego podejścia jest to, że gotowy produkt można realnie ocenić laboratoryjnie. Można sprawdzić:
- średni rozmiar cząstek,
- rozkład wielkości,
- stabilność układu,
- powtarzalność partii.
Innymi słowy: producent nie opiera się wyłącznie na założeniu, że układ „utworzy się później”, lecz może badać to, co faktycznie trafia do użytkownika.
Czym są proszki liposomalne
Produkty proszkowe opisywane jako liposomalne są najczęściej formą pośrednią. W technologicznym języku można je określać jako suche układy fosfolipidowe lub proliposomy.
Nie oznacza to automatycznie, że są bezwartościowe. Oznacza natomiast, że trzeba bardzo precyzyjnie rozumieć, czym są.
W takim produkcie zwykle znajduje się:
- składnik aktywny,
- fosfolipid lub mieszanina fosfolipidów,
- czasem stabilizatory lub substancje pomocnicze.
Po kontakcie z wodą układ ten może zacząć organizować się w różne struktury lipidowe. Problem polega na tym, że bez badania nie wiadomo dokładnie:
- czy rzeczywiście powstają liposomy,
- jaki mają rozmiar,
- jaka część układu to małe cząstki, a jaka większe agregaty,
- jak stabilna jest taka dyspersja.
To jest najważniejszy punkt całej dyskusji.
Co dzieje się po dodaniu wody do proszku liposomalnego
Wielu użytkowników zakłada, że jeśli produkt nazywa się liposomalny, to po dodaniu wody automatycznie powstanie stabilna, dobrze zorganizowana struktura liposomów. Technologicznie nie jest to takie proste.
Po uwodnieniu proszku mogą powstać różne układy:
- małe liposomy,
- większe liposomy,
- micele,
- agregaty lipidowe,
- zwykła emulsja,
- mieszanina kilku populacji cząstek.
I właśnie dlatego sama deklaracja „liposomalny proszek” nie mówi jeszcze zbyt wiele o końcowej jakości układu.
W praktyce wszystko zależy od:
- jakości fosfolipidów,
- stosunku składników,
- sposobu rekonstytucji,
- temperatury wody,
- czasu mieszania,
- stabilności układu po utworzeniu.
Jeśli producent nie pokazuje badań po uwodnieniu, użytkownik nie ma pewności, co tak naprawdę powstaje.
.
Dlaczego wielkość cząstek ma znaczenie
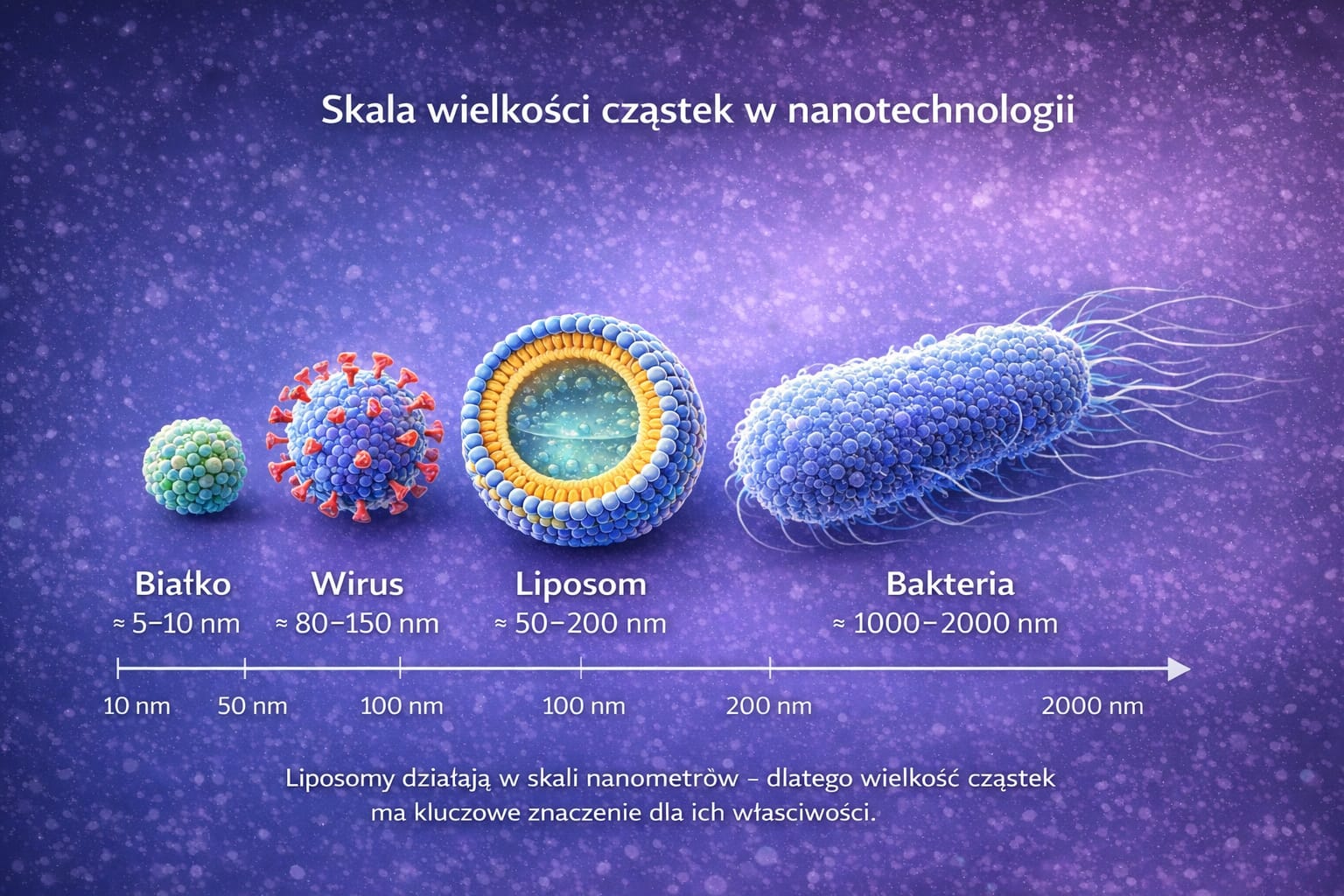
Rys.2 Porównanie wielkości liposomów (50–200 nm) z innymi strukturami biologicznymi w skali nanometrycznej.
W technologii liposomalnej i nanoemulsyjnej rozmiar cząstek jest jedną z najważniejszych cech całej formulacji. W przypadku ekstraktów roślinnych również można zauważyć duże różnice technologiczne między klasycznymi formami a formulacjami liposomalnymi.
Szerzej opisaliśmy to w artykule „Ziołowe suplementy liposomalne – czym różnią się od klasycznych ekstraktów?”.
To właśnie wielkość struktur lipidowych w dużym stopniu decyduje o właściwościach fizycznych układu oraz o tym, jak zachowuje się on w środowisku wodnym.
W przypadku formulacji liposomalnych mówimy najczęściej o strukturach o wielkości od kilkudziesięciu do kilkuset nanometrów. Jest to skala znacznie mniejsza niż większość struktur biologicznych, takich jak komórki czy bakterie.
Dla lepszego zrozumienia tej skali warto zauważyć, że:
- typowa komórka ma wielkość kilkunastu do kilkudziesięciu mikrometrów,
- bakterie mają zwykle około 1000–2000 nanometrów,
- wirusy często mieszczą się w zakresie 80–150 nanometrów.
Liposomy znajdują się więc w zakresie nanometrycznym, czyli w skali bardzo małych struktur biologicznych.
Powierzchnia cząstek i właściwości formulacji
Zmniejszanie wielkości cząstek powoduje bardzo duży wzrost ich całkowitej powierzchni.
Jeżeli tę samą ilość substancji rozdzielimy na bardzo wiele małych struktur zamiast kilku dużych agregatów, całkowita powierzchnia kontaktu z otoczeniem staje się znacznie większa.
W praktyce oznacza to między innymi:
- lepszą dyspersję w wodzie,
- bardziej stabilne rozproszenie składników,
- bardziej jednorodne właściwości fizykochemiczne formulacji.
Właśnie dlatego w wielu technologiach farmaceutycznych i nutraceutycznych dąży się do uzyskania jak najmniejszych i jednocześnie stabilnych cząstek.
Jednorodność układu ma równie duże znaczenie
Sama średnia wielkość cząstek nie mówi jednak wszystkiego o jakości formulacji.
Dwie próbki mogą mieć podobną średnią wielkość cząstek, na przykład około 120 nm, a mimo to zupełnie inną strukturę wewnętrzną.
W pierwszym przypadku większość cząstek może mieć bardzo podobny rozmiar, tworząc jednorodny układ lipidowy.
W drugim przypadku ta sama średnia wartość może wynikać z mieszanki:
- bardzo małych struktur lipidowych
- dużych agregatów tłuszczowych
- nieregularnych struktur micelarnych
Taki układ jest znacznie mniej stabilny i znacznie trudniejszy do przewidywania pod względem właściwości fizycznych.
Rozkład wielkości cząstek
Dlatego w analizie technologii liposomalnych niezwykle istotny jest nie tylko sam średni rozmiar cząstek, ale także rozkład ich wielkości w całej próbce.
Jeżeli większość struktur mieści się w wąskim zakresie wielkości, układ jest bardziej jednorodny i stabilny.
Jeżeli natomiast rozkład jest szeroki i w próbce pojawiają się zarówno bardzo małe cząstki, jak i duże agregaty lipidowe, formulacja może zachowywać się zupełnie inaczej niż sugerowałaby sama średnia liczba podana w nanometrach.
Z tego powodu w analizach technologicznych bardzo często ocenia się również parametr określający jednorodność układu, który pozwala określić, czy struktury lipidowe mają podobną wielkość.
Znaczenie wielkości cząstek w praktyce
W praktyce technologicznej różnice w wielkości cząstek mogą wpływać na wiele właściwości formulacji, między innymi na:
- stabilność układu w czasie,
- sposób rozpraszania w wodzie,
- odporność na agregację lipidów,
- jednorodność całej dyspersji.
Dlatego w przypadku technologii liposomalnych sama deklaracja „liposomalny” nie mówi jeszcze wiele o jakości formulacji.
Dwa produkty opisane w podobny sposób mogą mieć zupełnie inne właściwości technologiczne właśnie ze względu na różnice w rozmiarze i strukturze cząstek lipidowych.
Dlaczego potrzebne są badania laboratoryjne
Ponieważ struktury lipidowe mają rozmiar nanometryczny, nie można ich ocenić w prosty sposób wizualnie.
W większości przypadków dopiero odpowiednie metody analityczne pozwalają określić:
- wielkość cząstek,
- rozkład ich wielkości,
- jednorodność całego układu.
To właśnie dlatego w badaniach technologii liposomalnych stosuje się specjalistyczne metody laboratoryjne pozwalające analizować cząstki w skali nanometrycznej.
Jak bada się liposomy w praktyce
Jednym z najczęściej stosowanych badań w ocenie takich formulacji jest DLS, czyli Dynamic Light Scattering — po polsku dynamiczne rozpraszanie światła.

Rys.3 Schemat badania wielkości cząstek w formulacji liposomalnej przy użyciu metody DLS (Dynamic Light Scattering
Badanie to pozwala określić:
- średni rozmiar cząstek,
- rozkład wielkości,
- poziom jednorodności układu.
Często analizuje się także PDI (polydispersity index), czyli wskaźnik mówiący o tym, czy próbka zawiera cząstki o podobnych rozmiarach, czy raczej szeroką i chaotyczną mieszaninę.
To właśnie takie badania pozwalają odpowiedzieć na pytanie, czy dany układ rzeczywiście ma charakter nano-lipidowy, czy też jest po prostu mieszaniną większych struktur.
I tu dochodzimy do bardzo ważnego wniosku:
w przypadku proszku najważniejsze są badania wykonane po rekonstytucji, czyli po dodaniu wody.
Czy wszystkie produkty liposomalne są takie same
Zdecydowanie nie.
Pod wspólnym słowem „liposomalny” mogą kryć się bardzo różne rozwiązania technologiczne. Na końcowy efekt wpływają m.in.:
- rodzaj fosfolipidów,
- proporcje składników,
- sposób produkcji,
- stopień enkapsulacji,
- wielkość cząstek,
- stabilność układu.
Dlatego dwa produkty opisane tym samym słowem mogą działać zupełnie inaczej.
Jedna formulacja może być dobrze zorganizowaną i stabilną dyspersją o małych cząstkach, a inna jedynie układem, który teoretycznie ma utworzyć się po dodaniu wody, ale w praktyce daje szeroki rozkład i duże agregaty.
To nie jest kwestia samej nazwy. To kwestia jakości technologii.
Czy proszek liposomalny to to samo co płynny liposom ?
Nie.
To jest najkrótsza i najuczciwsza odpowiedź.
Płynny układ liposomalny jest gotową formulacją w środowisku wodnym, którą można zbadać i scharakteryzować jeszcze przed użyciem.
Proszek liposomalny najczęściej jest suchym układem fosfolipidowym, który dopiero po kontakcie z wodą może tworzyć struktury lipidowe. Ostateczny efekt zależy więc od procesu rekonstytucji i jakości samej technologii.
Nie oznacza to, że każdy proszek jest z definicji zły. Oznacza jednak, że wymaga znacznie większej ostrożności w ocenie.
Na co warto zwrócić uwagę przy wyborze suplementu liposomalnego
Jeśli chcemy spojrzeć na produkt bardziej świadomie, warto zwrócić uwagę na kilka rzeczy.
1. Czy producent opisuje technologię w sposób konkretny
Ogólne hasła marketingowe to za mało. Im więcej konkretów, tym lepiej.
2. Czy dostępne są badania wielkości cząstek
To jeden z najważniejszych parametrów w przypadku formulacji lipidowych.
3. Czy wiadomo, jak wygląda układ po rekonstytucji
To szczególnie ważne przy proszkach.
4. Jakie fosfolipidy zostały użyte
Jakość źródła lipidów ma duże znaczenie.
5. Czy produkt jest stabilny
Stabilność to nie dodatek marketingowy, ale jedna z podstawowych cech jakości.
Co to oznacza w praktyce dla użytkownika
Najważniejszy wniosek jest prosty:
nie każda forma opisana jako liposomalna musi oznaczać ten sam poziom zaawansowania technologicznego.
W świecie suplementów warto odróżniać:
- gotowy układ lipidowy w produkcie,
od - układu, który ma dopiero powstać po użyciu.
To rozróżnienie jest kluczowe, jeśli chcemy oceniać realną jakość produktu, a nie tylko jego nazwę.
Liposomalne suplementy roślinne — nowy kierunek rozwoju
Najciekawszy kierunek rozwoju technologii liposomalnej dotyczy dziś nie tylko klasycznych witamin, ale także związków roślinnych o niskiej rozpuszczalności i ograniczonej biodostępności.
To właśnie w tym obszarze formulacja ma często największe znaczenie. Dotyczy to zwłaszcza substancji, które w zwykłej formie są trudne do efektywnego wykorzystania przez organizm.
W takich przypadkach technologia nie jest tylko dodatkiem marketingowym. Staje się realnym narzędziem formulacyjnym.
Podsumowanie
Technologia liposomalna jest jednym z najciekawszych kierunków rozwoju współczesnych suplementów. Warto jednak patrzeć na nią precyzyjnie.
Najważniejsza różnica między formą płynną a proszkową polega na tym, że:
- w płynnej formulacji układ lipidowy istnieje już w gotowym produkcie,
- w proszku układ dopiero ma powstać po kontakcie z wodą.
A to oznacza, że w przypadku proszku kluczowe znaczenie mają badania wykonane po rekonstytucji — zwłaszcza analiza wielkości cząstek i stabilności.
Im bardziej rozwinięta technologia, tym mniej miejsca pozostaje na domysły, a więcej na realne parametry formulacji.
Najczęstsze pytania o suplementy liposomalne (FAQ)
Czy każdy suplement oznaczony jako liposomalny działa tak samo?
Nie. Określenie „liposomalny” odnosi się do sposobu formulacji, jednak w praktyce różnice technologiczne między produktami mogą być bardzo duże. Na końcowy efekt wpływają m.in. jakość fosfolipidów, wielkość cząstek, stabilność układu oraz sposób produkcji. Dlatego dwa produkty opisane jako liposomalne mogą znacząco różnić się właściwościami fizycznymi i zachowaniem w środowisku wodnym.
Czy proszek liposomalny po dodaniu wody zawsze tworzy liposomy?
Nie zawsze. W przypadku wielu produktów proszkowych mamy do czynienia z suchą mieszaniną składników, która dopiero po kontakcie z wodą może tworzyć struktury lipidowe. Ostateczny efekt zależy jednak od jakości technologii, proporcji składników oraz sposobu rekonstytucji. Dlatego w praktyce ważne jest, aby oceniać takie formulacje także po dodaniu wody.
Jak można sprawdzić jakość formulacji liposomalnej?
Jedną z najczęściej stosowanych metod jest analiza DLS (Dynamic Light Scattering), czyli dynamiczne rozpraszanie światła. Badanie to pozwala określić wielkość cząstek w próbce oraz ich rozkład. Dzięki temu można sprawdzić, czy w preparacie dominują struktury nano, czy też większe agregaty.
Dlaczego wielkość cząstek w formulacjach liposomalnych jest ważna?
Wielkość cząstek ma duży wpływ na właściwości fizyczne całego układu. Mniejsze i bardziej jednorodne cząstki zazwyczaj oznaczają większą powierzchnię kontaktu oraz lepszą stabilność dyspersji. Dlatego w technologii liposomalnej kontrola rozmiaru cząstek jest jednym z podstawowych parametrów jakości.
Czy liposomy występują również w naturze?
Tak. Struktury przypominające liposomy występują naturalnie w wielu układach biologicznych. Jednym z często podawanych przykładów jest mleko, w którym tłuszcze również występują w postaci mikroskopijnych struktur lipidowych otoczonych warstwą fosfolipidów. Pokazuje to, że organizmy żywe od dawna wykorzystują podobne mechanizmy transportu substancji.
Na co warto zwrócić uwagę przy wyborze suplementu liposomalnego?
Przy wyborze suplementu liposomalnego warto zwrócić uwagę na kilka elementów:
- czy producent opisuje technologię w sposób konkretny,
- czy dostępne są informacje o wielkości cząstek,
- czy formulacja była badana metodami laboratoryjnymi,
- jakie fosfolipidy zostały wykorzystane,
- czy produkt ma stabilną formulację w środowisku wodnym.
W praktyce właśnie na tym etapie pojawia się największa różnica między produktem marketingowym a realną technologią.
Dlatego coraz więcej marek decyduje się nie tylko na gotowe rozwiązania, ale na współpracę z producentem, który realnie kontroluje proces tworzenia formulacji liposomalnych.
Jeśli chcesz zobaczyć, jak wygląda produkcja i podejście technologiczne od środka, możesz sprawdzić tutaj:
produkcja suplementów liposomalnych
Im więcej transparentnych informacji o technologii, tym łatwiej ocenić rzeczywistą jakość produktu.
Czy nazwa „liposomalny” zawsze oznacza zaawansowaną technologię?
Nie zawsze. W praktyce określenie „liposomalny” bywa stosowane w bardzo szeroki sposób. Dlatego warto zwracać uwagę nie tylko na nazwę produktu, ale także na dane technologiczne oraz badania laboratoryjne potwierdzające strukturę i wielkość cząstek.
.
Jeśli ten temat jest dla Ciebie interesujący — zostaw swój e-mail.
Kategorie Wiedzy
Ostatnie posty


Technologia 50 Nanometrów – Nowy poziom biodostępności polifenoli

Kurkumina liposomalna-biodostępność, działanie i porównanie z wlewami




